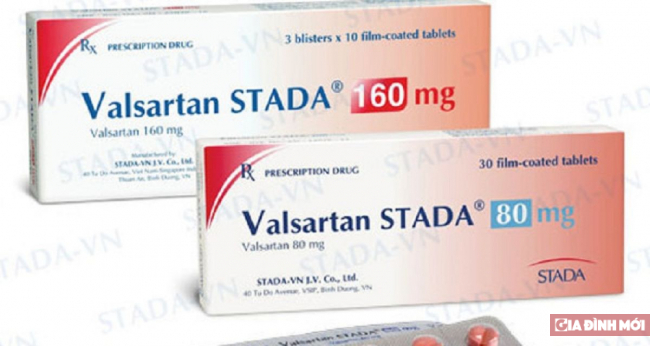
Cục Quản lý Dược thông báo thu hồi, ngừng sản xuất, ngừng nhập khẩu nguyên liệu và các thuốc có chứa valsartan được sản xuất từ nguyên liệu valsartan do các công ty Zhuhai Rundu Pharmaceutical Co, Ltd; Zheijang Tianyu Pharmaceutical Co. Ltd; Hetero Labs Itd sản xuất.
Cụ thể, những loại bị thu hồi gồm thuốc Valsartan 160 (Công ty cổ phần Dược phẩm Cửu Long); thuốc Cobidan 80 (Công ty cổ phần BV Pharma); 5 loại thuốc gồm Meyervasid M, Mayervas 160, Mayervas 80, Mayervasid, Meyervasid F, của Công ty liên doanh Meyer-BPC; thuốc Valthotan F11m Coated Tablets 160mg Standard (Công ty Standard ChemPharm Co., Ltd).
Quyết định này căn cứ vào thông báo của cơ quan Quản lý dược phẩm châu Âu (EMA), cơ quan Quản lý dược Mỹ, cơ quan Quản lý dược Đài Loan (Trung Quốc) và một số cơ quan quản lý dược khác trên thế giới đã công bố thêm các nhà sản xuất nguyên liệu Valsartan chứa tạp chất N-nitrosodimethylamine (NDMA).
Thuốc chứa hoạt chất Valsartan được sử dụng để điều trị cao huyết áp, suy tim và sau nhồi máu cơ tim.
Như vậy, tính đến nay, đã có 39 loại thuốc trong nước và 15 loại thuốc thành phẩm từ nước ngoài có hoạt chất Valsartan bị đình chỉ lưu hành và thu hồi do phát hiện tạp chất có nguy cơ gây ung thư.
H.NBạn đang xem bài viết Bộ Y tế: Thu hồi thêm 8 loại thuốc tim mạch nhiễm tạp chất gây ung thư bị thu hồi tại chuyên mục Sức khỏe Cộng đồng của Gia Đình Mới, tạp chí chuyên ngành phổ biến kiến thức, kỹ năng sống nhằm xây dựng nếp sống gia đình văn minh, tiến bộ, vì bình đẳng giới. Tạp chí thuộc Viện Nghiên cứu Giới và Phát triển (Liên Hiệp Các Hội Khoa học Kỹ thuật Việt Nam), hoạt động theo giấy phép 292/GP-BTTTT. Bài viết cộng tác về các lĩnh vực phụ nữ, bình đẳng giới, sức khỏe, gia đình gửi về hòm thư: bankhoahoc@giadinhmoi.vn.
Tin liên quan
 Tags:
Tags: