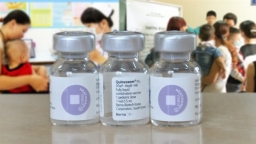
vắc-xin ComBe Five được chuyển đổi sau khi có thông tin nhà sản xuất vắc-xin Quinvaxem ngừng sản xuất
Mới đây, Bộ Y tế thông tin, vì nhà sản xuất là Công ty Berna Biotech ngừng sản xuất vắc-xin Quinvaxem nên Bộ Y tế đã có kế hoạch chuyển đổi vắc-xin mới.
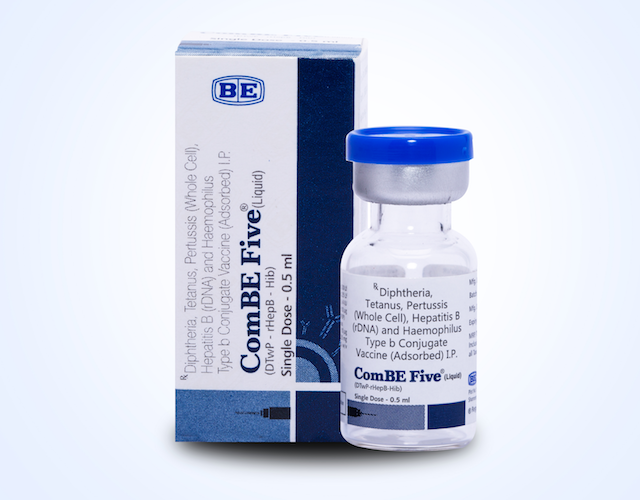
Theo đó, vắc-xin ComBe Five được Bộ y tế cấp phép lưu hành ở Việt Nam từ tháng 5/2017, vắc-xin có thành phần tương tự Quinvaxem có hiệu quả phòng 5 loại bệnh: bạch hầu, ho gà, uốn ván, viêm gan B, viêm phổi/viêm màng não do vi khuẩn Hib. Trong đó, thành phần ho gà là toàn tế bào.
Trước lo ngại về độ an toàn của vắc-xin mới, Bộ Y tế chia sẻ, từng lô vắc xin khi nhập khẩu vào Việt Nam đều được Viện Kiểm định Quốc gia Vắc-xin - Sinh phẩm Y tế kiểm định và đạt an toàn trước khi đưa vào chương trình tiêm chủng mở rộng.
Vắc-xin này có dạng trình bày tương tự như vắc-xin Quinvaxem: đóng 1 lọ/ liều và lọ vắc-xin có gắn chỉ thị nhiệt độ để giám sát việc tiếp xúc với nhiệt độ của từng lọ vắc-xin trong quá trình bảo quản, vận chuyển trước khi sử dụng. Về tính an toàn và hiệu quả, ComBe Five tương tự các vắc-xin 5 trong 1 có cùng thành phần.
Theo Bộ Y tế, vắc-xin này đã đạt tiêu chuẩn thẩm định của WHO và đã được sử dụng ở hơn 43 quốc gia với hơn 400 triệu liều. Nhiều quốc gia cũng sử dụng vắc-xin này trong chương trình tiêm chủng mở rộng.
PGS TS Trần Như Dương - Phó Viện trưởng Viện Vệ Sinh Dịch tễ cho biết, ngay tại Ấn Độ - nước sở tại, hơn 130 triệu liều ComBe Five đã được sử dụng trong chương trình tiêm chủng mở rộng. Mọi tiêu chuẩn, cách sử dụng đều tương tự Quinvaxem nên thuận lợi cho các cán Bộ Y tế áp dụng.
Kết quả sử dụng tại thực địa 4 huyện của tỉnh Hà Nam năm 2016 ghi nhận, vắc-xin ComBe Five cũng có một số những phản ứng nhất định sau tiêm. Trong đó, phản ứng thông thường xuất huyện vào ngày thứ nhất sau tiêm vắc-xin bao gồm phản ứng tại chỗ tiêm đau, 5-15% quầng đỏ, 34-39% sốt, không ghi nhận bất cứ phản ứng nghiêm trọng nào sau tiêm.
Riêng với hơn 130 triệu liều đã sử dụng tại Ấn Độ, ghi nhận 11 trường hợp phản ứng nặng sau tiêm chủng trong đó có 5 trường hợp sốt cao, khóc dai dẳng, nôn... và đều qua khỏi không có biến chứng. Ngoài ra, có 6 ca tử vong sau tiêm là những phản ứng nặng nhất. Tuy nhiên, qua kiểm tra, thẩm định đánh giá có: 1 trường hợp viêm phổi, 2 trường hợp sặc sữa, 1 trường hợp do nhiễm trùng huyết nặng, 1 trường hợp không rõ nguyên nhân, 1 trẻ do có hội chứng đột tử trẻ sơ sinh. Từ đó, kết luận cho thấy, tất cả trường hợp tử vong đều không liên quan đến chất lượng vắc-xin.
GS.TS Đặng Đức Anh - Viện trưởng Viện Vệ sinh Dịch tễ TƯ cho biết, dự kiến chuyển đổi sử dụng vắc-xin ComBe Five sẽ được triển khai trên toàn quốc trong tháng 6-7/2018. Trước khi triển khai toàn quốc, dự án tiêm chủng mở rộng sẽ triển khai tại Hà Nam, Bình Định, Kon Tum, Đồng Tháp.
Cũng theo ông Anh, số vắc-xin Quinvaxem còn lại vẫn được sử dụng cho tới khi thay thế bằng vacxin mới. Lịch tiêm chủng không thay đổi, trẻ dưới 1 tuổi cần tiêm đủ 3 mũi. Trẻ đã tiêm Quinvaxem vẫn có thể tiếp tục tiêm ComBe Five.
Vắc-xin phối hợp 5 trong 1 phòng các bệnh bạch hầu, ho gà, uốn ván, viêm gan B và viêm phổi/viêm màng não mủ do vi khuẩn Hib: Trong hơn 7 năm qua, Chương trình TCMR đã sử dụng vắc-xin Quinvaxem để tiêm cho trẻ dưới 1 tuổi. Hiện nay, nhà sản xuất Berna Biotech đã ngừng sản xuất vắc-xin Quinvaxem, số vắc-xin Quinvaxem còn lại dự kiến sẽ sử dụng đến hết tháng 5/2018 trên quy mô toàn quốc.
Vì vậy, Bộ Y tế đã có kế hoạch chuyển đổi sử dụng vắc-xin Quinvaxem bằng loại vắc-xin phối hợp 5 trong 1 tương tự về thành phần và hiệu quả phòng bệnh.
Theo kế hoạch, vắc-xin ComBe Five sẽ được đưa vào sử dụng trên quy mô nhỏ tại 04 tỉnh, sau đó sẽ đưa vào sử dụng rộng rãi trên quy mô toàn quốc vào cuối quý II năm 2018.
Vắc-xin Quinvaxem vẫn tiếp tục được sử dụng trong chương trình TCMR cùng với việc chuyển đổi sử dụng loại vacxin phối hợp 5 trong 1.
Hồng Ngọc/GiaDinhMoiBạn đang xem bài viết Loại vắc-xin nào sẽ thay thế Quinvaxem trong chương trình tiêm chủng mở rộng 2018? tại chuyên mục Sống khỏe của Gia Đình Mới, tạp chí chuyên ngành phổ biến kiến thức, kỹ năng sống nhằm xây dựng nếp sống gia đình văn minh, tiến bộ, vì bình đẳng giới. Tạp chí thuộc Viện Nghiên cứu Giới và Phát triển (Liên Hiệp Các Hội Khoa học Kỹ thuật Việt Nam), hoạt động theo giấy phép 292/GP-BTTTT. Bài viết cộng tác về các lĩnh vực phụ nữ, bình đẳng giới, sức khỏe, gia đình gửi về hòm thư: [email protected].
Tin liên quan
 Tags:
Tags: